-
O copiar el link



Filtros de Contribuciones
Buscar Contribución:
PorMagda Rocío Gómez Marroquín*, Sandra L Carmona, Diana Burbano David, Andrea del Pilar Villarreal, Mauricio Soto Suárez, Adriana González Almario
Recibido: 15/junio/2025 – Publicado: 29/abril/2026
DOI: https://doi.org/10.18781/R.MEX.FIT.2401-3
Resumen Antecedentes/Objetivo. Las sustancias bioactivas como fosfitos y silicio representan una alternativa promisoria para el manejo de la marchitez vascular del tomate, debido a su potencial para inhibir el crecimiento del patógeno e inducir mecanismos de defensa en la planta. El objetivo de este estudio fue evaluar el efecto de tres fuentes de fosfitos y una fuente de silicio sobre el aislamiento Fol59 de Fusarium oxysporum f. sp. lycopersici raza 2 mediante ensayos in vitro e in planta.
Materiales y Métodos. En condiciones in vitro, se determinó el porcentaje de inhibición del crecimiento radial (PICR) del aislamiento Fol59 de Fusarium oxysporum f. sp. lycopersici raza 2 en medio PDA suplementado con cada sustancia bioactiva en concentraciones entre 10 y 20 000 ppm, bajo un diseño completamente al azar (4 × 9), con cuatro tratamientos y nueve concentraciones, cinco réplicas técnicas y tres biológicas. En condiciones in planta, se evaluó el Área Bajo la Curva del Progreso de la Enfermedad (ABCPE) y el porcentaje de eficacia mediante un diseño completamente al azar (4 × 2), con cuatro tratamientos y dos concentraciones, considerando cuatro condiciones experimentales: control, control inoculado, tratamientos sin inoculación y tratamientos inoculados. Se utilizaron 20 unidades experimentales por tratamiento y tres réplicas biológicas.
Resultados. A los siete días, las sustancias bioactivas redujeron el crecimiento radial del hongo entre 70 y 100 %, con diferencias significativas entre las concentraciones. La mayor inhibición se registró con silicio a 10 000 ppm (100 %), seguido de fosfito de calcio a 2 000 ppm (99.4 %) y fosfito de potasio a 20 000 ppm (99 %). En ensayos in planta, a los 14 días después de inoculación, el control presentó una incidencia del 100 % y una severidad del 98 %. En contraste, el tratamiento con fosfito de potasio (KPhi1) a 2 000 ppm redujo la severidad al 56 %, lo que representa una eficacia del 42 % en comparación con el control.
Conclusión. Los fosfitos y el silicio mostraron un efecto inhibitorio sobre el crecimiento micelial del hongo bajo condiciones in vitro. En ensayos in planta, el fosfito de potasio, a 2 000 ppm fue el tratamiento más eficaz, reduciendo severidad de la marchitez vascular causada por Fol59.
PorLeandris Argentel Martínez, Ofelda Peñuelas Rubio*, Francisco Cervantes Ortíz, Joe Luis Arias Moscoso, Francisco Cadena Cadena, Pamela Romo Rodríguez, Lorenzo Pérez López, Rosario Alicia Fierro Coronado
Recibido: 15/enero/2026 – Publicado: 29/abril/2026
DOI: https://doi.org/10.18781/R.MEX.FIT.2601-2
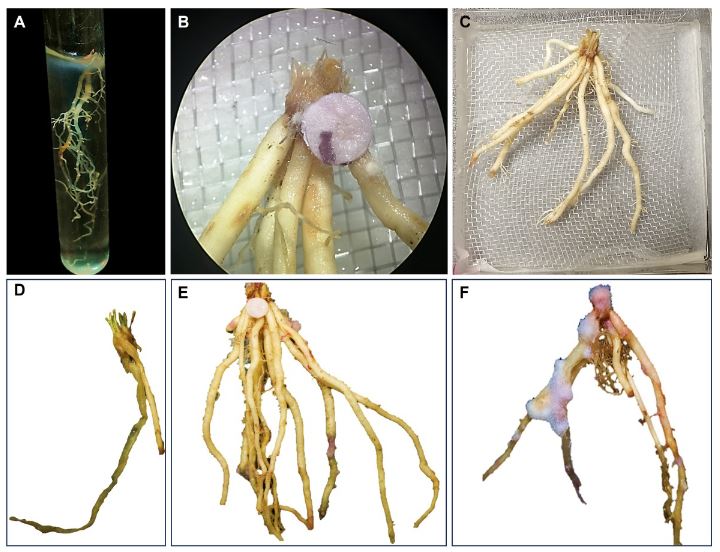
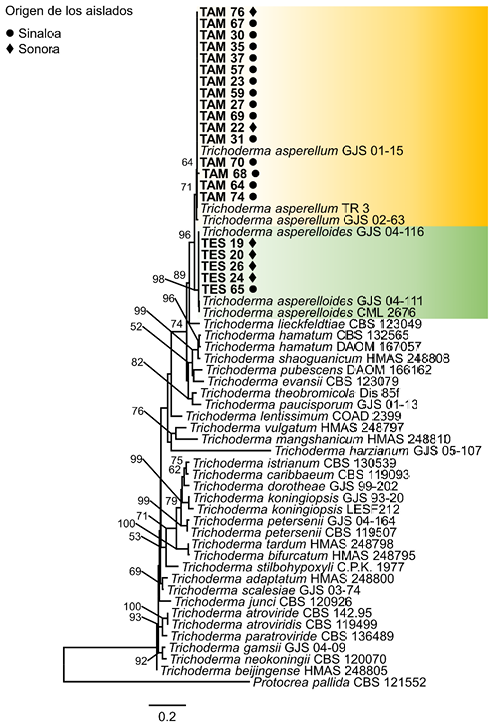
Resumen Antecedentes/Objetivo. El género Fusarium comprende algunos de los hongos fitopatógenos más importantes que afectan al cultivo de maíz, ya que ocasionan enfermedades como la pudrición de la raíz, tallo y mazorca, que afectan la productividad agrícola de este cultivo. En la búsqueda de alternativas agrobiotecnológicas para el control de este hongo, se desarrolló el presente estudio para evaluar el potencial antagonista de rizobacterias de Parkinsonia aculeata contra cepas de Fusarium spp. asociadas a maíces criollos del Bajío, México.
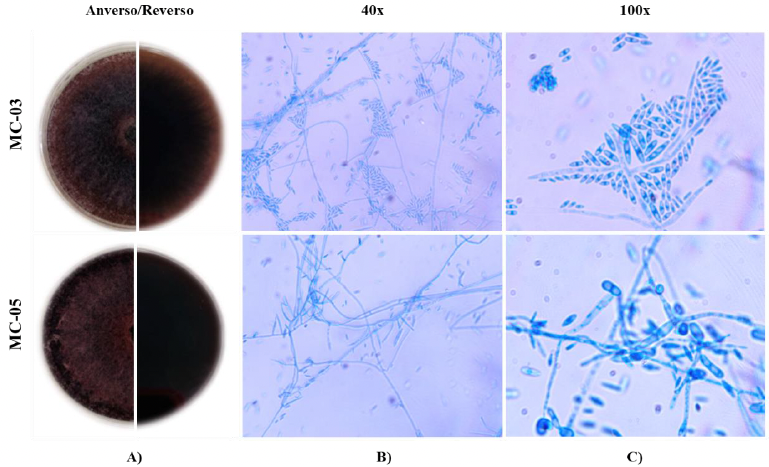
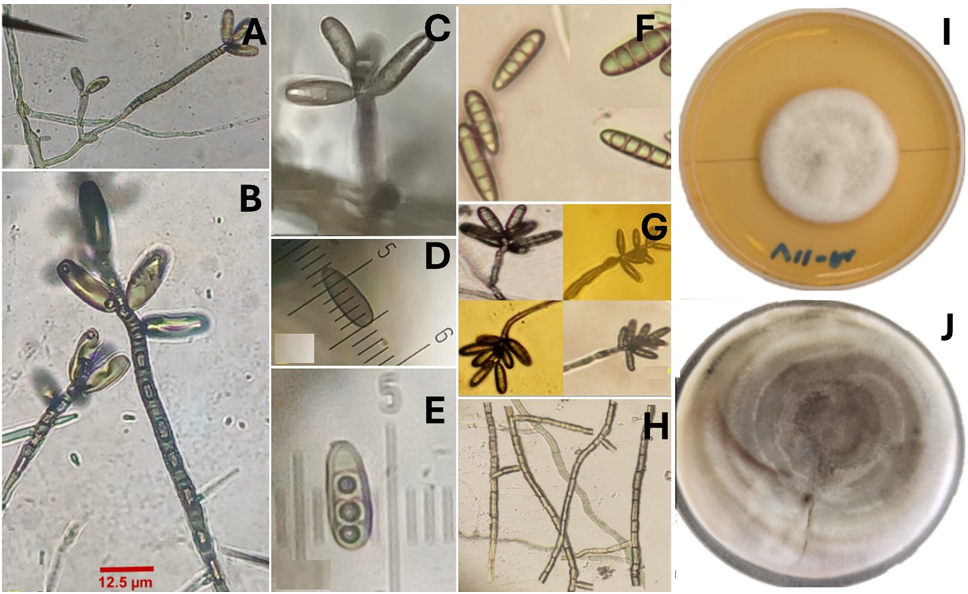
Desarrollo experimental. Se emplearon dos cepas de Fusarium spp. (MC-03 y MC-05), aisladas de raíces de maíces nativos del Bajío, México con síntomas de Fusariosis. Estos hongos se confrontaron in vitro con nueve rizobacterias de P. aculeata: Enterobacter cloacae (BA1), Priestia megaterium (BA4 y BA-7B), Sinomonas halotolerans (BA10-B), BP5 (Staphylococcus warneri), BP6 (P. endophytica), Bacillus subtilis (TP1 y TP2) y S. hominis (TM6). Se realizó una caracterización micro-macroscópica de las cepas fúngicas y bioquímica para las rizobacterias. Se determinó la inhibición del crecimiento radial de los aislados fúngicos mediante confrontaciones duales hongo-rizobacterias por triplicado. Se empleó un diseño completamente aleatorizado, analizando los datos obtenidos en el software STATISTICA mediante una ANOVA basada en un modelo lineal de efectos fijos y una prueba comparación de medias por DMS (p>0.05).
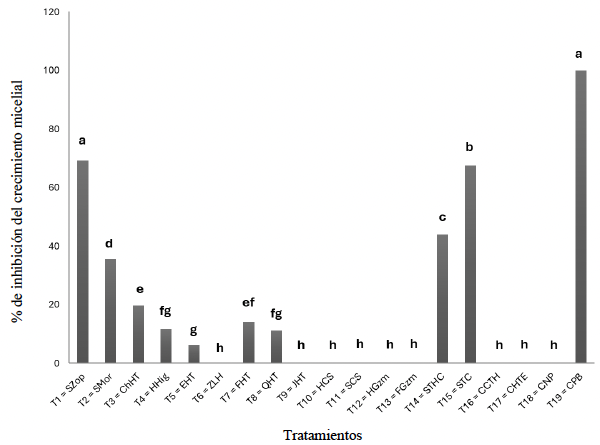
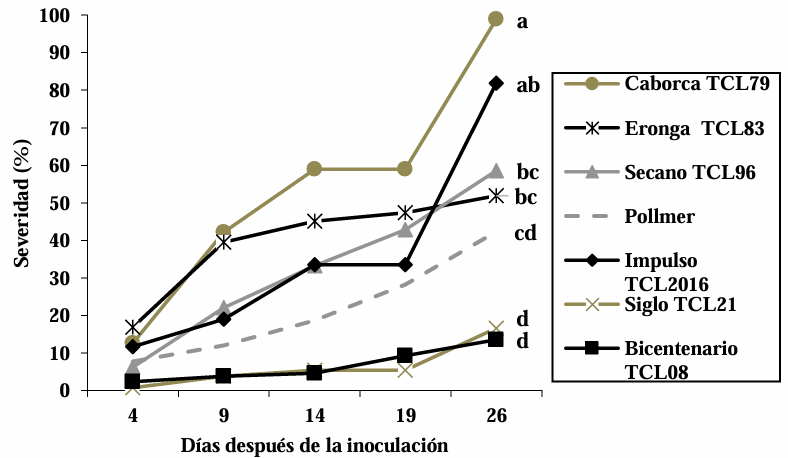
Resultados. A excepción de P. endophytica (BP6), todas las rizobacterias presentaron actividad enzimática relacionada con mecanismos de antagonismo fúngico. B. subtilis (TP1) produjo gluacanasas, lipasas y proteasas. La caracterización micro y macroscópica de las cepas fúngicas indicó que pertenecen a Fusarium spp. En la confrontación rizobacterias- MC-03, las cepas bacterianas de B. subtilis (TP1 y TP2) fueron estadísticamente iguales y lograron la mayor inhibición del crecimiento micelial (23 %). Con la cepa fúngica MC-05, P. endophytica (BP6) y S. hominis (TM6) fueron estadísticamente superiores al resto de las rizobacterias al momento inhibir el crecimiento micelial en 17 %, seguidas por las dos cepas de B. subtilis (TP1 y TP2) que inhibieron el 10 y 17 % respectivamente.
Conclusión. Existió variabilidad significativa en la respuesta del crecimiento micelial de los hongos ante las rizobacterias. B. subtilis (TP1 y TP2), S. hominis (TM6) y P. endophytica (BP6), presentaron un efecto antagónico, ya que inhibieron el crecimiento micelial de las cepas de Fusarium spp. hasta en 23 % respecto al control absoluto y comercial. El presente estudio establece las bases científicas preliminares para la obtención de un biofungicida con capacidades específicas de inhibición de los hongos estudiados.
Detección de un potencial alphanucleorhabdovirus infectando Carica papaya en Costa Rica
PorLaura Garita Salazar, William Villalobos Muller, Mauricio Montero Astúa, Antonio Bogantes Arias, Teresita Coto Morales, Izayana Sandoval Carvajal, Lisela Moreira Carmona*
Recibido: 11/febrero/2026 – Publicado: 29/abril/2026
DOI: https://doi.org/10.18781/R.MEX.FIT.2602-3
Resumen Antecedentes/Objetivo. Clorosis foliar, entrenudos cortos, y pecíolos curveados con estrías color púrpura se observan en plantaciones de papaya (Carica papaya) en las regiones Norte y Atlántica en Costa Rica desde el 2014. La identificación de un presunto virus de plantas asociado con estos síntomas fue el objetivo de esta investigación.
Desarrollo experimental. El tejido vegetal fue evaluado mediante ELISA (cuatro virus de plantas y el género potyvirus), microscopia electrónica de transmisión (MET), RT-PCR (con iniciadores universales para virus de plantas), secuenciación y análisis filogenéticos.
Resultados. Todas las pruebas de ELISA resultaron negativas. Mediante MET, se observaron sólo en las plantas sintomáticas, partículas virales con forma de bala, éstas dentro de membranas en los núcleos y el citoplasma. Amplicones de 900 pb se obtuvieron consistentemente en las muestras sintomáticas usando iniciadores degenerados para rhabdovirus de plantas. Las secuencias nucleotídicas mostraron similitudes entre 95.6 y 96.8 % con un alphanucleorhabdovirus (Alphanucleorhabdovirus, Rhabdoviridae) tentativo que infecta papaya.
Conclusión. Este es el primer reporte de un alphanucleorhabdovirus tentativo asociado con plantas sintomáticas de papaya mostrando la enfermedad del "pecíolo rayado", como se le conoce localmente en Costa Rica, pero los postulados de Koch deben ser cumplidos y el vector identificado.
PorCynthia Ford Villalón, David Schneider, Idalia Montesinos Solano, Jimena Carrillo Tripp*
Recibido: 13/diciembre/2025 – Publicado: 23/abril/2026
DOI: https://doi.org/10.18781/R.MEX.FIT.2512-4
Resumen Antecedentes/Objetivo. El virus de la mancha roja de la vid, GRBV (Grablovirus vitis) afecta el cultivo de vid (Vitis vinifera) causando pérdidas económicas significativas. En México, donde el GRBV se ha reportado en regiones vitivinícolas como Baja California, la información sobre los posibles vectores de GRBV es limitada. Aunque el periquito tricornudo de la alfalfa (Spissistilus festinus) es un vector confirmado en los Estados Unidos de América, el papel de otros membrácidos en viñedos a nivel global aún no está claro. Recientemente, el membrácido neártico (Tortistilus wickhami) ha sido reportado en Baja California, lo que motivó este estudio para evaluar su potencial para adquirir y transmitir el GRBV.
Desarrollo experimental. Entre febrero y noviembre de 2023, se recolectaron adultos del membrácido neártico en 20 viñedos del Valle de Guadalupe, Baja California. Un total de 30 individuos fue analizado por PCR en tiempo real para detectar GRBV. En mayo, 2024, se recolectaron 17 individuos adicionales que fueron utilizados en ensayos de transmisión, con un periodo de acceso a la adquisición de hasta cuatro días en hojas de vid (cv. Cabernet Sauvignon) infectadas con GRBV, seguido de un periodo de acceso a la inoculación de hasta 9 días en hojas libres de virus. Los insectos y las hojas receptoras fueron analizados por PCR en tiempo real para detectar GRBV.
Resultados. El virus GRBV fue detectado en 6.7 % (2/30) de los individuos colectados en 2023, los cuales provenían exclusivamente de viñedos previamente confirmados como positivos a GRBV. En los ensayos de transmisión, el 53 % (9/17) de los insectos adquirieron partículas virales tras alimentarse de hojas infectadas; sin embargo, no hubo infección detectable en ninguna de las hojas receptoras.
Conclusión. Este estudio demuestra que el membrácido neártico, un insecto filogenéticamente cercano y morfológicamente similar al periquito tricornudo de la alfalfa (vector confirmado de GRBV), fue capaz de adquirir el virus tanto en condiciones de campo como en laboratorio; no obstante, bajo las condiciones experimentales de laboratorio probadas, no se demostró la transmisión a plantas receptoras.
PorSebastian Iglesias Osores*, Luis A Alvarez
Recibido: 08/diciembre/2025 – Publicado: 23/abril/2026
DOI: https://doi.org/10.18781/R.MEX.FIT.2512-2
Resumen Antecedentes/Objetivo. El oídio del arándano, asociado a Erysiphe vaccinii, es una enfermedad foliar que puede provocar defoliación y afectar el desempeño del cultivo. En Perú, la información sobre el uso foliar de ácido peracético para su manejo en campo es limitada. El objetivo del presente estudio fue evaluar el efecto de aplicaciones foliares de ácido peracético al 15 % sobre la incidencia de oídio en arándano bajo condiciones de campo en Ica, Perú.
Desarrollo experimental. El ensayo se realizó en un cultivo comercial de arándano cv. Biloxi en Ica, Perú, bajo un diseño de bloques completos al azar con cinco tratamientos: testigo sin aplicación y ácido peracético al 15 % a 2, 4, 6 y 8 mL L-1, con cuatro repeticiones. Los tratamientos se aplicaron por vía foliar en dos oportunidades separadas por siete días, con un volumen de 600 L ha-1. La variable de respuesta fue la incidencia de hojas con síntomas de oídio (con inoculación natural), evaluada en siete fechas desde la primera aplicación. También se registró visualmente la presencia de síntomas de fitotoxicidad.
Resultados. Antes de la primera aplicación no se detectaron diferencias entre tratamientos. Después de la primera aplicación, el ácido peracético redujo la incidencia de oídio respecto al testigo, con eficacias iniciales de hasta 67.7 %. Tras la segunda aplicación, las dosis de 4, 6 y 8 mL L-1 mostraron la mejor respuesta, con eficacias máximas de 69.3, 78.0 y 79.7 %, respectivamente. La dosis de 2 mL L-1 presentó un efecto menor. En ninguna de las dosis evaluadas se observaron síntomas visibles de fitotoxicidad.
Conclusión. En las condiciones de este ensayo, el ácido peracético al 15 % redujo la incidencia foliar de oídio en arándano, con mejor respuesta en las dosis de 4, 6 y 8 mL L-1 (69.3, 78.0 y 79.7 %). Estos resultados indican un efecto favorable del producto bajo condiciones de campo, aunque su validación requiere evaluaciones adicionales en más localidades o campañas.
PorMiguel Salvador Figueroa, José Fernando Gómez López, Miguel Salvador Adriano, María de Lourdes Adriano Anaya, Isidro Ovando Medina, Benjamín Moreno Castillo*
Recibido: 26/agosto/2025 – Publicado: 11/marzo/2026
DOI: https://doi.org/10.18781/R.MEX.FIT.2408-4
Resumen Antecedentes/Objetivo. La producción y calidad del cultivo de jitomate (Solanum lycopersicum) se ven fuertemente reducidas por el hongo Fusarium oxysporum, agente causal de la fusariosis. Convencionalmente se aplican fungicidas químicos, aunque ante infecciones severas las cosechas se pierden en su totalidad. Las condiciones ambientales favorables incrementan los niveles de incidencia, capacidad de infección y de diseminación. El control biológico es una estrategia útil para combatir este tipo de patógenos. El objetivo de esta investigación consistió en determinar la incidencia de fusariosis (Fusarium oxysporum) en plantas de tomate cultivadas en campo y tratadas con Trichoderma asperellum Jc01 y Bacillus subtilis ANT01.
Desarrollo experimental. Trichoderma asperellum Jc01 y Bacillus subtilis ANT01 de manera individual y en combinación, fueron aplicados semanalmente a la zona de goteo de plantas de tomate (Solanum lycopersicum). Periódicamente se muestreó la incidencia de la enfermedad tanto en las plantas tratadas y no tratadas para monitorear la evolución de la incidencia de la enfermedad durante 15 semanas. Adicionalmente se registró el número de flores y frutos producidos en las plantas experimentales.
Resultados. Al final del ensayo de campo, las plantas tratadas con B. subtilis ANT01 mostraron 60 % menos incidencia con respecto al testigo y un total de 47.9 frutos producidos planta-1, mientras que las plantas tratadas con Trichoderma asperellum Jc01 o la combinación de ambos microorganismos mostraron 16 y 28 % menos incidencia que el testigo, y 18.0 y 27.3 frutos producidos planta-1, respectivamente.
Conclusión. Los resultados muestran evidencia parcial del potencial de la cepa ANT01 como agente de biocontrol de F. oxysporum en plantas de tomate.
PorGuillermo Ascencio Luciano, Nicolás Maldonado Moreno, Reinaldo Méndez Aguilar, Moisés Felipe Victoriano*
Recibido: 21/agosto/2024 – Publicado: 06/marzo/2026
DOI: https://doi.org/10.18781/R.MEX.FIT.2408-00
Resumen Antecedentes/Objetivo. El cultivo de soya es afectado por diversas enfermedades ocasionadas por hongos, éstos pueden reducir los rendimientos hasta en un 100 %. El objetivo de este trabajo fue identificar el hongo asociado a la mancha foliar en soya, y evaluar la influencia de la humedad del suelo en la incidencia y severidad de la enfermedad en planta y hoja en 30 genotipos de soya.
Materiales y Métodos. Se colectaron tres hojas de soya con síntomas de mancha foliar por genotipo, para su identificación morfológica del hongo mediante claves taxonómicas. Se evaluaron dos condiciones de humedad (riego y temporal). La incidencia en planta se estimó a partir de 10 plantas al azar, en el mismo periodo se evaluó la incidencia y severidad foliar; para incidencia foliar se contaron hojas sanas y hojas enfermas de 10 plantas por genotipo. Posteriormente, a 10 plantas por genotipo se les seleccionó una hoja en la quinta posición de arriba abajo, las hojas se fotografiaron, y se calculó el área dañada y área total de la hoja con el programa ImageJ, con lo que se determinó severidad en hoja.
Resultados. Se identificó a Alternaria alternata asociado a la mancha foliar. En el ambiente de temporal la incidencia en hoja por A. alternata osciló entre 4.4 al 50.55 %, para la severidad los valores oscilaron entre 0.3 y 17.4 %. En el ambiente de riego la incidencia varió entre 7 a 50.9 %, la severidad osciló entre 0 y 24.7 %.
Conclusión. Se asoció A. alternata a la mancha foliar en soya, la cual es poco estudiada en México, y actualmente se desconocen sus efectos en este cultivo, por ello resulta de interés científico seguir trabajando en proyectos de investigación con esta especie.
Diseño y validación de una escala diagramática para evaluar la severidad del mildiú del pepino
PorJuan Carlos Gonzalez Acevedo, Santiago Domínguez Monge*, Dagoberto Guillen Sánchez, Víctor López Martínez, Porfirio Juárez López, Irán Alia Tejacal, Julio David Mendoza García
Recibido: 05/enero/2026 – Publicado: 06/marzo/2026
DOI: https://doi.org/10.18781/R.MEX.FIT.2601-1
Resumen Antecedentes/Objetivo. El mildiu del pepino (Cucumis sativus), causado por Pseudoperonospora cubensis, es una de las principales enfermedades foliares que afectan la producción de pepino en Morelos, México. Debido a la ausencia de métodos estandarizados y validados para la cuantificación de la severidad de esta enfermedad, el objetivo de este estudio fue diseñar y validar una escala diagramática para su evaluación.
Desarrollo experimental. Se desarrolló una escala diagramática compuesta por ocho niveles de severidad (2, 4, 8, 16, 24, 32, 40 y 47 % de área foliar afectada), a partir de hojas naturalmente infectadas cuya severidad real fue determinada mediante análisis digital de imágenes con el software Assess®. La validación de la escala se realizó con la participación de 20 evaluadores, quienes estimaron visualmente la severidad de 50 hojas con diferentes niveles de daño en tres evaluaciones sucesivas: una sin ayuda de la escala (SA) y dos con ayuda de la escala, realizadas a las dos (CA1) y cuatro semanas (CA2) posteriores a la primera evaluación.
Resultados. El uso de la escala diagramática incrementó significativamente la precisión de las estimaciones de severidad, con coeficientes de correlación de Pearson de r = 0.91 y r = 0.93 en CA1 y CA2, respectivamente, en comparación con la evaluación sin escala (r = 0.34). Asimismo, el sesgo generalizado fue menor cuando se utilizó la escala (Cb > 0.9), lo que se reflejó en una mayor concordancia general entre las estimaciones visuales y los valores reales de severidad (ρc > 0.9).
Conclusión. La escala diagramática desarrollada es una herramienta confiable, precisa y reproducible para la estimación de la severidad del mildiu en pepino bajo condiciones de campo.
PorVíctor Manuel Arzola Mora, Héctor Eduardo Villaseñor Mir, Salvador Carranza González*, Carlos Sánchez Abarca, René Hortelano Santa Rosa, Julio Huerta Espino, María Elsa Rodríguez Contreras, Pawan Kumar Singh, Xinyao He
Recibido: 14/octubre/2025 – Publicado: 02/marzo/2026
DOI: https://doi.org/10.18781/R.MEX.FIT.2510-3
Resumen Antecedentes/Objetivo. El tizón de la espiga (fusariosis), ocasionado por Fusarium graminearum en trigo harinero, reduce el rendimiento del cultivo y contamina el grano con micotoxinas como el deoxinivalenol (DON), lo que afecta la calidad e inocuidad del producto. Su severidad ha aumentado en zonas cálidas y húmedas durante la floración, lo que destaca la necesidad de contar con estrategias de manejo integrado. El presente estudio tuvo como objetivo evaluar la interacción entre tres genotipos de trigo (Heilo, Falcin y Ocoroni F86) y tres fungicidas (Tilt® 250 EC (propiconazol al 25 %), Nativo® 300 SC [trifloxistrobin (20 %) + tebuconazol (10 %)); y Folicur® 250 EW (tebuconazol (25 %)], con el fin de reducir la severidad de F. graminearum y mejorar el rendimiento bajo condiciones de campo durante dos ciclos de producción.
Desarrollo experimental. El experimento se realizó en el Campo Experimental Valle de México del INIFAP durante los ciclos primavera-verano 2022 y 2023, se utilizó un diseño de parcelas divididas con tres repeticiones. Se registraron variables agronómicas como días a floración (DF), días a madurez (DM), altura de planta (ALT), rendimiento de grano (REND) y severidad de F. graminearum en la espiga (FEsp). El análisis estadístico se llevó a cabo mediante ANOVA, prueba de Duncan (p<0.05) y correlaciones de Pearson.
Resultados. La variedad Heilo, cuando se aplicó propiconazol (25 %) o trifloxistrobin (20 %) + tebuconazol (10 %), mostró el mayor rendimiento (>4 000 kg ha⁻¹) y la menor severidad de fusariosis (FEsp ≤1.5). En contraste, Ocoroni F86 fue susceptible, incluso bajo tratamiento químico. Las condiciones climáticas tuvieron un efecto significativo en la severidad de la enfermedad.
Conclusión. El uso combinado de variedades con resistencia genética y fungicidas triazoles componen una estrategia agronómica factible para mitigar la fusariosis. Se recomienda validar estos resultados en distintos ambientes para ampliar su aplicabilidad.
PorEdith Luna Martínez, Sergio Aranda Ocampo*, Dimas Mejía Sánchez, Candelario Ortega Acosta, Manuel Livera Muñoz, Laura Delia Ortega Arenas, Antonio Mora Aguilera, Eligio Pérez Sosa, Daniel Telìz Ortiz
Recibido: 08/diciembre/2025 – Publicado: 25/febrero/2026
DOI: https://doi.org/10.18781/R.MEX.FIT.2512-3
Resumen Antecedentes/Objetivo. El cultivo de pitahaya (Selenicereus undatus) se ha extendido en los últimos años en México. En 2023, en huertos comerciales de pitahaya en el estado de Puebla se observaron síntomas de pudrición de tallo. El objetivo fue caracterizar e identificar el agente causal de la pudrición del tallo, evaluar la patogenicidad del agente causal en diferentes especies de pitahaya, además de otras especies de plantas y su sensibilidad in vitro a formulaciones de bactericidas comerciales.
Materiales y Métodos. Se analizaron 10 tallos con pudrición provenientes de Huitziltepec, Puebla. Muestras de tejido de cada tallo se desinfestaron y se maceraron en 500 μL de agua destilada estéril; de aquí, se sembraron 100 μL en medio de cultivo Wilbrink´s y B de King. Del crecimiento bacteriano, la cepa CPHU23 se caracterizó bioquímicamente y se identificó por análisis multilocus de secuencias (MLSA, por sus siglas en inglés) y filogenético de los genes rpoB, gyrB, leuS, y fusA. La patogenicidad de CPHU23 se evaluó por infiltración de 3 × 10⁸ UFC mL⁻¹ en cinco especies del género Selenicereus: S. ocamponis, S. purpusi, Selenicereus sp. “Golden”, Selenicereus sp. “Solferina” y S. undatus, así como en Agave cupreata, A. angustifolia, Aloe vera, Allium cepa, Solanum lycopersicum y Capsicum annuum. La sensibilidad in vitro se determinó por el método de difusión en disco con 10 formulaciones de bactericidas comerciales.
Resultados. De los 10 tallos se aislaron tres morfotipos bacterianos. El morfotipo CPHU23 fue el más frecuente con colonias amarillas, redondas, borde liso, aspecto mucoide. La caracterización bioquímica de la cepa CPHU23 mostró 93 % de similitud con Pantoea vagans. El análisis MLSA agrupó filogenéticamente al aislamiento CPHU23 dentro del clado Pantoea vagans filogenéticamente relacionadas a las cepas tipo de P. vagans LMG 24199, YI-1 y MA I6050 con soporte de bootstrap superior a 85 %. La inoculación de P. vagans CPHU23 causó pudrición de tallo en las cinco especies del género Selenicereus, en hojas de A. cupreata y A. vera, pero no en bulbos de A. cepa y frutos de S. lycopersicum y C. annuum. Pantoea vagans CPHU23 fue sensible in vitro a oxicloruro de cobre, sulfato de gentamicina, clorhidrato de oxitetraciclina y estreptomicina, pero resistente a kasugamicina.
Conclusión. Pantoea vagans es el agente causal de la pudrición de tallo en pitahaya en Puebla. Las cinco variedades de pitahaya son susceptibles a la pudrición del tallo. Agave cupreata y Aloe vera podrían ser hospedantes potenciales de P. vagans. El uso de oxicloruro de cobre puede ser una estrategia eficiente de manejo de P. vagans en el cultivo de pitahaya en México.